新規抗がん薬 オニバイド®︎点滴静注とは?

この記事は、オニバイドについてまとめた記事です。
「オニバイドの名前は聞いてことあるけど、どんな特徴があるの?」
「オニバイドを投与するまたは投与している患者に関わっているけど、どんなことに注意したらいいの?」
そのオニバイドに関する疑問を解決できる記事となっています。
[author_box label=”この記事を書いた人]
オニバイドの概要
がん化学療法後に増悪した切除不能な膵癌に対して承認された新規抗がん薬です。
がん化学療法後に増悪した切除不能な膵癌なので、二次治療以降で投与可能です。
承認時は膵癌に対する適応のみとなっています。
膵癌においてイリノテカンは、FOLFIRINOXでしか投与できませんでした。しかしFOLFIRINOXは副作用の観点から高齢患者やPSが低い患者に対しては適応しづらいということがありました。
オニバイド®︎点滴静注の特徴
- イリノテカン塩酸塩水和物のリポソーム製剤
- 循環血中で長時間滞留する
- 腫瘍細胞内でのイリノテカン活性代代謝物の暴露期間延長
イリノテカンのおさらい
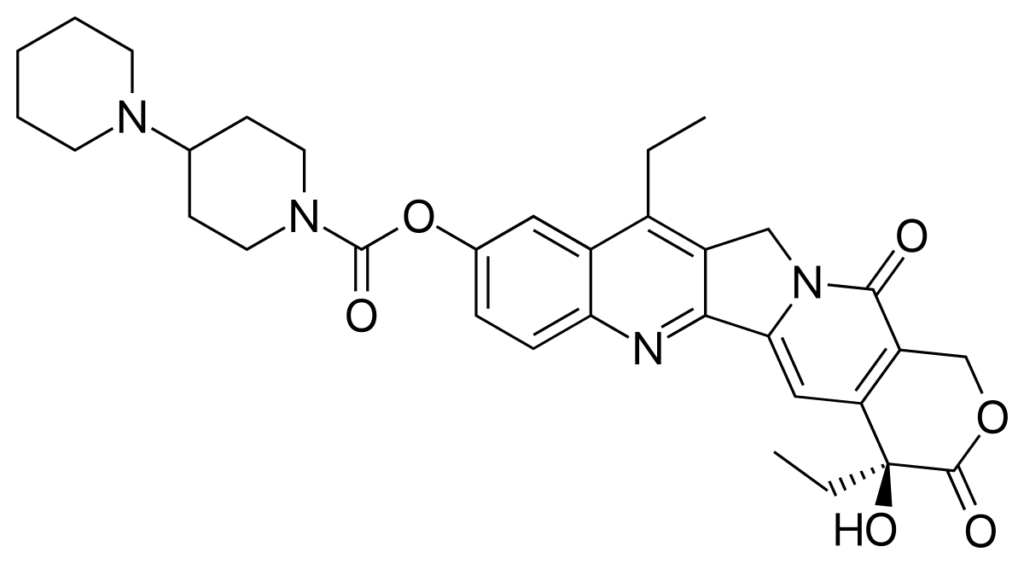
抗腫瘍性アルカロイドであるカンプトテシンから合成された抗悪性腫瘍薬です。
作用機序としては、トポイソメラーゼⅠ阻害薬に分類されます。
DNAの複製時に生じるねじれを解消するために単鎖切断・再結合を行うのがトポイソメラーゼで、これを阻害することでDNAの複製が抑制されて抗悪性腫瘍作用を示します。
リポソーム製剤にすることでどんなメリットがあるのか。
オニバイド®︎は有効成分のイリノテカンをリポソームのナノ粒子に封入したリポソーム製剤です。
では、リポソーム化することでどんなメリットがあるでしょうか。
- リポソームへの封入による血漿中循環時間の延長
- 血管透過性および滞留性亢進(EPR)効果に伴う腫瘍への集積
- 腫瘍内でのSNー38の暴露期間の延長による抗腫瘍活性の増強
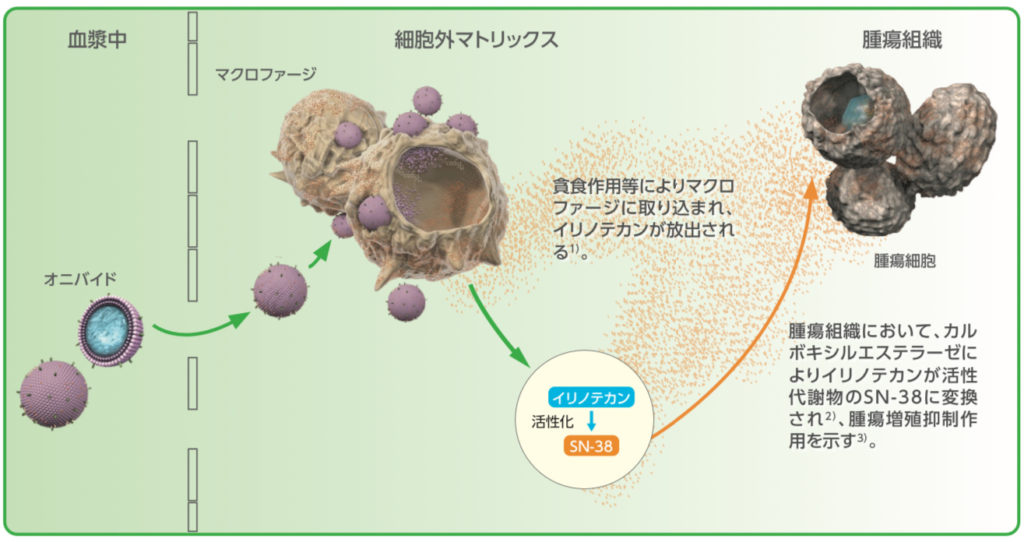
リポソーム化したことで、通常のイリノテカンの約1/5の投与量で同程度の血漿中、腫瘍内のSN−38濃度を示すとのことです。
臨床試験
海外第Ⅲ相試験(NAPOLI−1試験)

5-FU/LVにオニバイドを併用することで、OS(Overall Suevival:全生存期間)が4.2ヵ月から6.1ヵ月へ有意に延長することが示されました。
国内第Ⅱ相試験(331501試験)においても同等の結果となっています。
注意すべき副作用は?
主な副作用
50%以上:悪心
5〜50%未満:嘔吐、口内炎、便秘、無力症、発熱、食欲減衰、低カリウム血症、味覚異常、脱毛症、体重減少など
重大な副作用
- 骨髄抑制
- 好中球減少(44.8%)
- 白血球減少( 35.0%)
- 貧血(17.8%)
- 血小板減少(9.2%)
- 発熱性好中球減少症(2.5%)
- 無顆粒球症(0.6%)
- 汎血球減少症(0.6%)
- 下痢(49.7%)
- 感染症(10.4%)
- 肝機能障害(11.0%)、黄疸
- infusion reaction(4.9%)
- 血栓塞栓症( 1.2%)
- 腸炎( 1.2%)、腸閉塞( 0.6%)、消化管出血
- 播種性血管内凝固
- 間質性肺疾患
- 急性腎障害( 1.8%)
- 心筋梗塞、狭心症
- 心室性期外収縮
下痢
オニバイド®︎投与患者に対して、特徴的な副作用として下痢があります。
オニバイドによる下痢には早発型と遅発型の2種類あります。
早発型下痢
オニバイド投与中もしくは直後から24時間以内で発現する下痢です。
原因としては主にコリン作動性で、対応としては抗コリン薬を投与することで症状を緩和することができます。
コリン作動性症状として下痢症状のほかに、腹痛や、分泌液過多、鼻炎、発汗などがあります。
よく使われる抗コリン薬は、ブチルスコポラミン(ブスコパン®︎)があります。
ブチルスコポラミンは内服、注射薬があります。
投与中に症状がある場合は、注射で投与できますし、予防的に投与することも可能です。
外来化学療法後に自宅で症状が出た場合は、内服薬で対応することができます。
遅発型下痢
オニバイド投与24時間以降に発現する下痢です。
イリノテカンの活性代謝物SN−38による腸管粘膜障害によるものと考えられています。
対応としてはロペラミド(ロペミン®︎)を投与します。
用法用量
オニバイド®︎添付文書では、
フルオロウラシルおよびレボホリナートとの併用において、通常、成人にはイリノテカンとして1回70mg/m2(体表面積)を90分かけて2週間間隔で点滴静注する。なお、患者の状態により適宜減量する。
となっています。
投与スケジュールは以下のようになります。
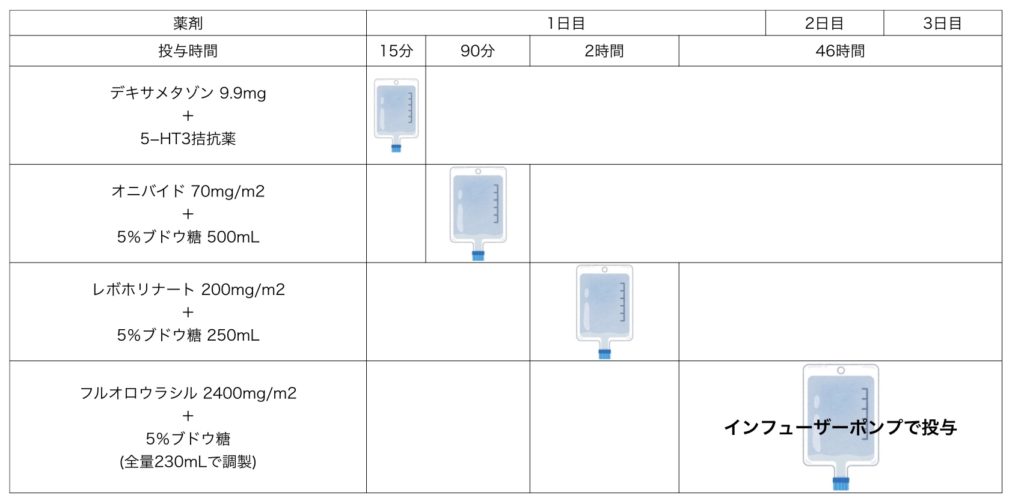
大腸がんにおけるFOLFIRIのイリノテカンがオニバイドに置き換わった感じですね。
CVポート造設が必要な点は、デメリットの一つです。
UGT1A1の遺伝子多型の確認を!
イリノテカンの活性代謝物にSN−38の代謝にUGT1A1が関与しています。
UGT1A1の遺伝子多型を有する患者ではSN−38の代謝が減少し、重篤な副作用をの発現リスクが上昇します。
そのため、UGT1A1の遺伝子多型の検査を行い、事前に副作用発現のリスクを把握することが大切です。
UGT1A1の遺伝子多型を有する患者に対しての投与量は、50mg/m2として開始します。
遺伝子多型に注意が必要な点は、既存のイリノテカン製剤と同様ですね。
まとめ
オニバイドについてまとめると、
1. 切除不能膵癌の二次治療以降で投与できるイリノテカン製剤である。
2. 注意すべき副作用は下痢があり、早発型と遅発型がある。
3. UGT1A1の遺伝子多型を確認すること!
参考
オニバイド®︎点滴静注 適正使用ガイド